Une RÉVOLUTION
médicale
déjà en marche
Une révolution dans plusieurs domaines thérapeutiques
Le développement de ces biotechnologies a permis des avancées majeures dans plusieurs pathologies.
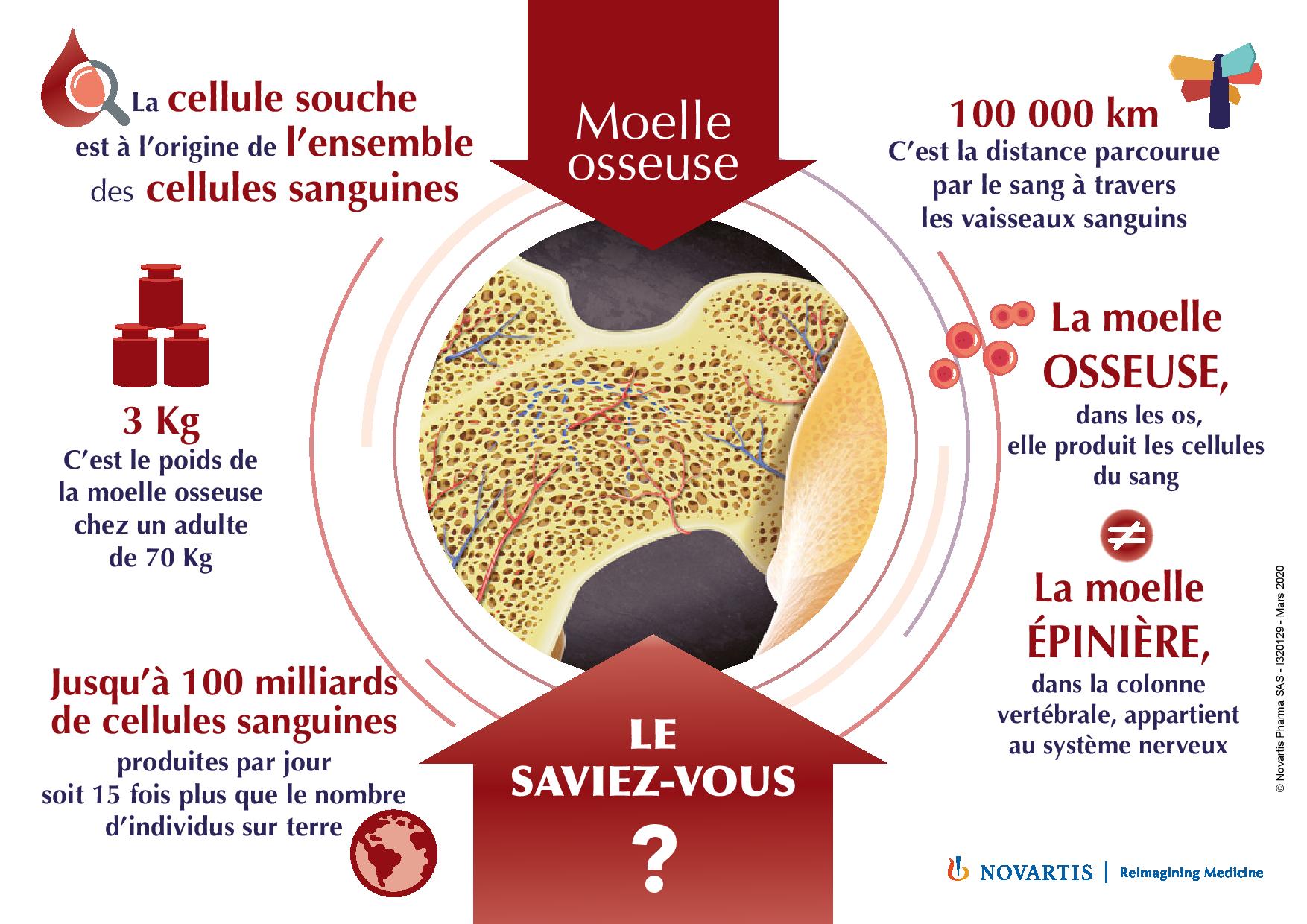
Dès les années 70, la thérapie cellulaire a rendu possible l'utilisation de cellules souches de la peau chez les grands brûlés, et les 1res greffes de moelles osseuse ont été réalisées dans les années 80.
Aujourd'hui, plusieurs traitements sont déjà sur le marché en hématologie, ophtalmologie, neurologie, gastro-entérologie et dermatologie.
Découvrez les pathologies bénéficiant déjà de traitements autorisés par thérapie génique ou cellulaire
Cliquez sur chaque aire thérapeutique
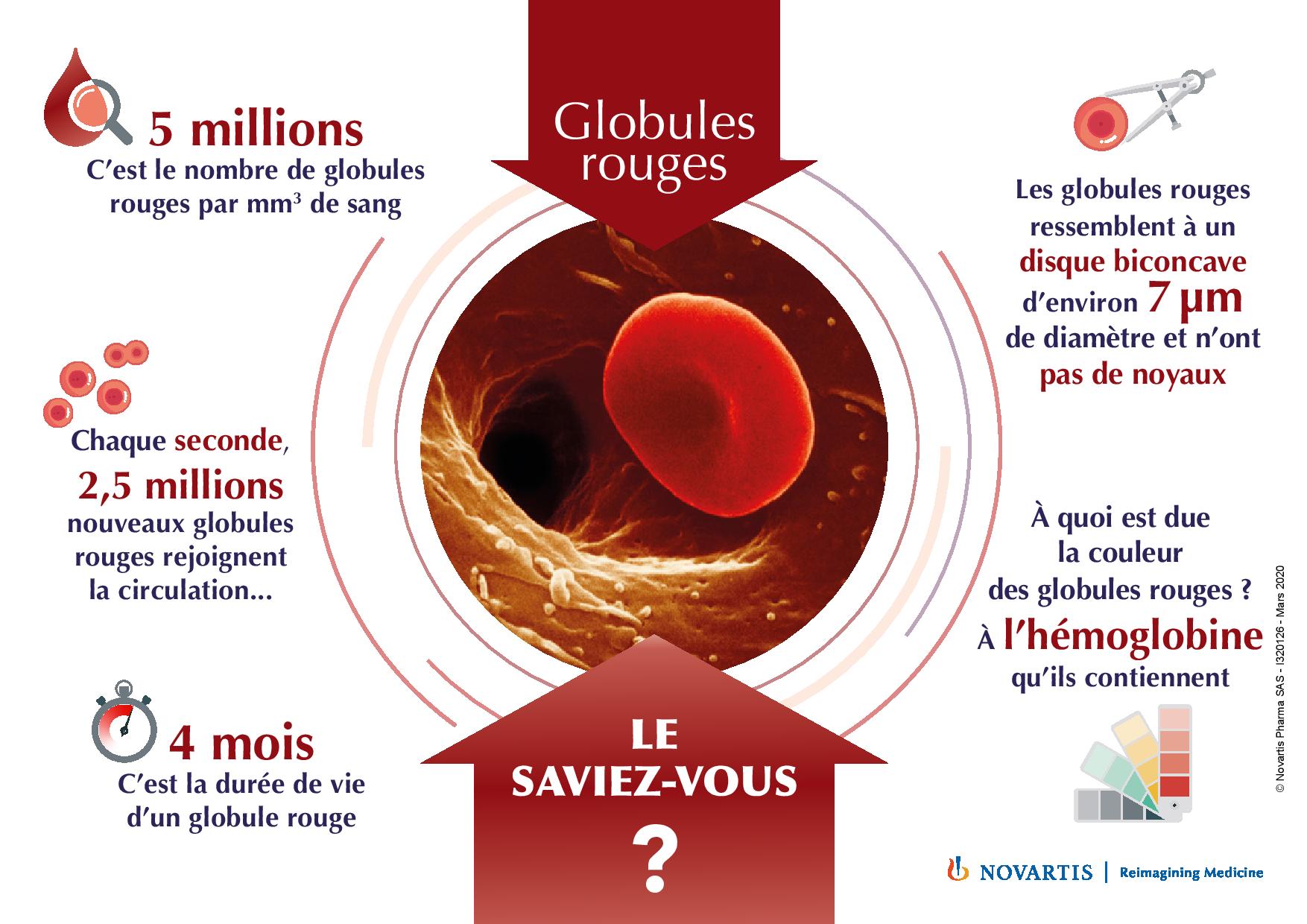
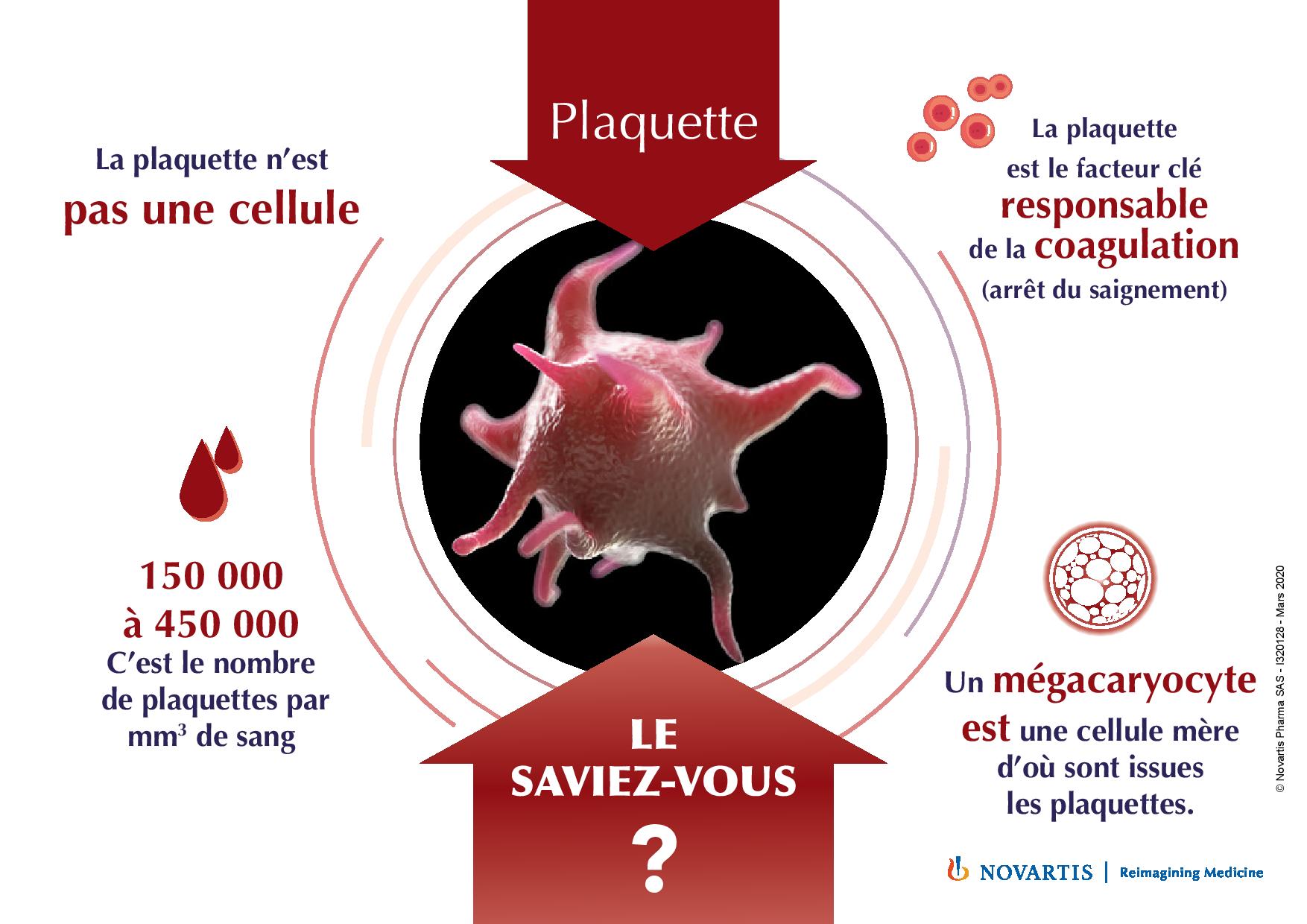
Cancers qui se développent à partir des cellules du sang (globules rouges, globules blancs, plaquettes). Ils sont dus à des altérations de ces cellules survenant à différents stades de leur maturation et qui favorisent leur prolifération. On distingue 3 grandes familles de cancers du sang :
- Leucémies, caractérisées le plus souvent par la présence de cellules anormales circulant dans le sang ;
- Myélomes, qui se manifestent notamment par des lésions osseuses ;
- Lymphomes, qui touchent principalement les ganglions.
En 2018, les cancers du sang, appelés hémopathies malignes, ont touché environ 45 000 personnes (25 000 hommes et 20 000 femmes). Cela correspond à environ 12 % de l'ensemble des nouveaux cas de cancer.
En savoir plus sur les différents types de cancers du sang
Leucémies : maladie qui se caractérise par la fabrication anormale des cellules sanguines par la moelle osseuse. Ces cellules anormales, appelées cellules leucémiques, sont créées en grande quantité et prolifèrent dans la moelle osseuse. Elles se répandent ensuite dans la circulation sanguine et peuvent atteindre tous les organes. Il existe plusieurs types de leucémies, selon la rapidité d’évolution de la maladie et le type de cellule touché.
Selon la rapidité d’évolution, on distingue les :
- Leucémies aiguës : évolution très rapide. Les cellules anormales ne parviennent pas à maturité et s’accumulent dans la moelle osseuse. Les symptômes apparaissent rapidement et le traitement doit être débuté le plus vite possible.
- Leucémies chroniques : évolution plus lente. Les cellules anormales ont le temps d’arriver à maturité.
Selon la lignée cellulaire atteinte, on distingue les :
- Leucémies lymphoïdes ou lymphoblastiques : elles atteignent les globules blancs, appelés lymphocytes. Les cellules anormales sont des lymphoblastes. Selon l’évolution, on différencie la leucémie lymphoïde aiguë (LLA) et la leucémie lymphoïde chronique (LLC). La LLA est la forme la plus répandue de leucémie aiguë chez les jeunes enfants tandis que la LLC affecte principalement les adultes.
- Leucémies myéloïdes : les cellules touchées sont celles de la lignée myéloïde (des cellules qui se transforment normalement en globules rouges, globules blancs ou plaquettes). La leucémie myéloïde aiguë (LMA) connait une évolution rapide tandis que la leucémie myéloïde chronique (LMC) connaît une évolution plus lente. Ces deux maladies touchent majoritairement le sujet adulte.
La LLC et les LMC sont les formes les plus fréquentes, avec plus de 3 000 (LLC) et plus de 4 000 (LMC) nouveaux cas en 2018.
Myélomes : cette pathologie touche un type particulier de globules blancs, appelés plasmocytes. Ils correspondent au stade final de spécialisation des lymphocytes B, et ont pour mission de produire des anticorps, afin de défendre l’organisme contre un agent infectieux. Lorsqu’un plasmocyte devient tumoral, il se multiplie de façon anormale et ne produit plus qu’un seul type d’anticorps, ce qui a pour effet de dérégler les autres plasmocytes. En conséquence, la capacité de notre organisme à se défendre contre les infections diminue. Ces plasmocytes tumoraux peuvent aussi envahir la moelle osseuse et réduire la formation d’autres cellules du sang. Les symptômes les plus spécifiques sont des douleurs et une fragilité osseuse, qui sont dues à la destruction de l’os par les plasmocytes tumoraux. Le myélome multiple est le type de cancer du sang le plus fréquent, avec plus de 5 000 nouveaux cas en 2018.
Lymphomes : ils se caractérisent par la prolifération excessive des globules blancs (lymphocytes B et T) au niveau des organes (ganglions, foie, rate), ce qui entraîne une augmentation de leur taille. Les principaux symptômes consistent donc en une augmentation de la taille des ganglions. Les lymphomes représentent plus de la moitié des cancers du sang. Plus de 16 000 nouveaux cas de lymphomes ont été recensés en 2018.
Maladie génétique qui touche les globules rouges et qui entraîne un transport d’oxygène insuffisant dans le sang. Les β-thalasssémies sont de sévérité variable : certaines formes n’entraînent aucun symptôme et d’autres mettent la vie en danger.
La β-thalassémie touche surtout les personnes originaires du pourtour méditerranéen (Corse, Italie, Sardaigne, Sicile, Grèce, Afrique du Nord), du Moyen-Orient, d’Asie (Chine, Inde, Vietnam, Thailande) et d’Afrique noire. Elle touche autant les hommes que les femmes. En France, on estime que 350 personnes sont atteintes de formes sévères dont près de 70 % sont des formes majeures.
En savoir plus sur la ß-thalassémie
La ß-thalassémie est une maladie qui touche l’hémoglobine, une protéine présente dans les globules rouges et qui donne au sang sa couleur rouge. L’hémoglobine a pour rôle de transporter l’oxygène et de le redistribuer à tout l’organisme. Elle est constituée de 4 « briques », appelées chaînes (2 alpha et 2 bêta) d’hémoglobine, qui sont assemblées entre elles. La ß-thalassémie est due à une mutation du gène bêta-globine. En conséquence, les chaînes bêta sont produites en quantité insuffisante ou nulle, ce qui entraîne une production insuffisante d’hémoglobine. Lorsque l’organisme ne peut pas compenser le déficit en hémoglobine, en fabricant de nouveaux globules rouges, il y a un déficit en globules rouges : c’est l’anémie.
Il existe environ 200 mutations différentes du gène bêta-globine responsables de la ß-thalassémie.
Déficit immunitaire combiné sévère (DICS)
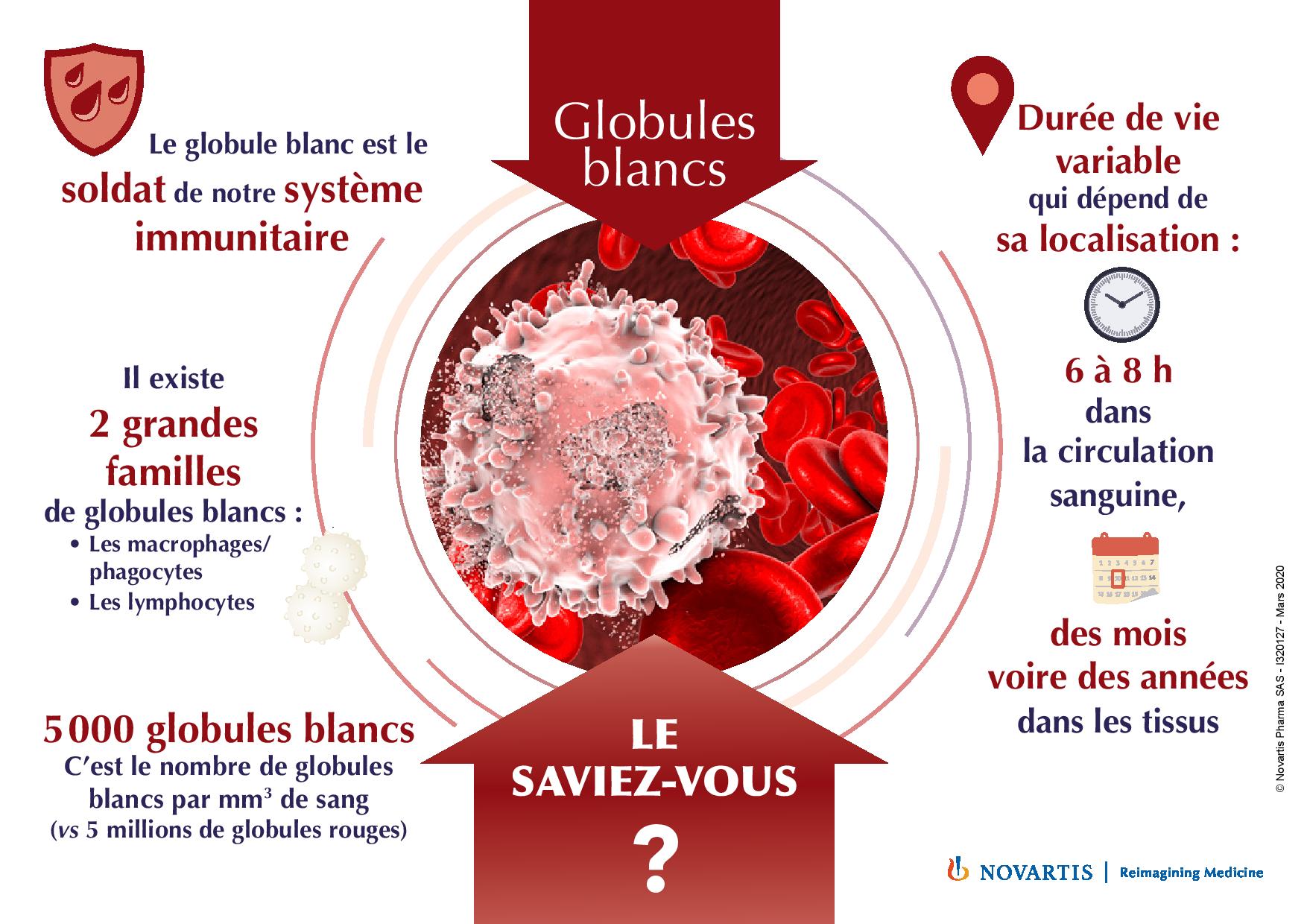
Le DICS est une pathologie rare qui touche la production ou le fonctionnement des globules blancs. Cela rend l’organisme incapable de se défendre contre les infections, ce qui se traduit notamment par un nombre excessif d’infections graves dès les premiers mois de la vie.
En savoir plus sur les DICS
Il existe différentes formes de DICS, dont les 3 plus fréquentes sont :
DICS liée à l’X : c’est la forme la plus fréquente, qui représente 45 à 50 % des cas de DICS. Elle est provoquée par une mutation qui touche un gène du chromosome X, responsable de la production d’un composant essentiel au fonctionnement des lymphocytes T.
DICS-ADA : forme qui représente environ 15 % des cas de DICS. Elle est liée à une mutation dans un gène se trouvant sur le chromosome 20. Ce gène permet la production d’une enzyme essentielle à la survie des lymphocytes T (adénosine désaminase, ADA). L’absence de cette enzyme entraîne la mort des lymphocytes T.
DICS-Jak3 : forme qui représente environ 10 % des DICS. La mutation touche cette fois un gène du chromosome 19, responsable de la production d’un composant essentiel au fonctionnement des lymphocytes T.
Pour certaines maladies du sang, le traitement consiste à effectuer une greffe de moelle osseuse. Cela permet aux patients de pouvoir se reconstituer un sang « neuf », en cas de destruction de la moelle osseuse par la maladie ou les traitements. Le risque lié à cette greffe est que la moelle osseuse du donneur ne reconnaisse pas l’organisme du receveur. À l’inverse, il se peut également que la moelle osseuse qui a été greffée rejette le corps du receveur, qui lui est étranger.
Les dystrophies rétiniennes héréditaires (DRH) représentent un groupe de maladies rares affectant la rétine. Ces pathologies sont dues à l’altération (mutation) de gènes (plus de 250 à ce jour) impliqués dans le fonctionnement et la régulation des cellules de la rétine. Elles entraînent par conséquent une perte progressive et graduelle de la vision pouvant évoluer vers la cécité.
Les DRH toucheraient environ 1 personne sur 40 000. Elles peuvent survenir de manière plus ou moins précoce, chez le nouveau-né, le jeune enfant ou l’adolescent.
Découvrez à travers ce film, le quotidien d'un jeune patient atteint de Dystrophies Rétiniennes Héréditaires
Il existe différents types de DRH et donc différents tests que les médecins peuvent effectuer pour déterminer celle dont vous souffrez.
Quels sont les signes et les symptômes de la DRH ?
En dehors des problèmes liés à la vision, vous pourrez rencontrer une multitude de signes et de symptômes différents. Ceux-ci varient en fonction de la forme de DRH. Retrouvez ci-dessous la liste de certains problèmes de vision rencontrés dans différents types de DRH qui pourraient nécessiter la mise en place d’autres tests par votre médecin.
Chez les bébés et les jeunes enfants :
- Nystagmus (mouvement incontrôlé des yeux)
- Photophobie (sensibilité à la lumière)
- Les yeux qui piquent et le besoin de les frotter
- Problèmes d’audition et d’équilibre (fréquemment associés au syndrome d’Usher)
Chez les enfants plus âgés et les adolescents :
- Difficulté à lire et à voir de loin
- Perte de l’acuité visuelle
- Cécité nocturne ou problèmes de vue lors de faible luminosité
- Faible réactivité des yeux lors du passage d’une forte luminosité à une plus faible
Comment sont diagnostiqués les DRH ?
Être diagnostiqué d’une DRH peut être déstabilisant, mais connaître le processus de diagnostic est essentiel à la compréhension des différentes options qui s’offrent à vous.
Vous pouvez rencontrer deux types de diagnostic : le diagnostic clinique et le diagnostic génétique.
Diagnostic clinique
Ce diagnostic est basé sur les différents symptômes que vous rencontrez ainsi que sur les tests effectués en cabinet médical. Le but est d’établir, à travers plusieurs tests effectués par votre médecin ou ophtalmologue, un premier diagnostic de la DRH. Ainsi vous pourrez savoir de quelle forme de DRH il s’agit et quelles sont les évolutions possibles.
Diagnostic génétique
Il est utilisé pour déterminer quelle mutation génétique cause votre DRH. Il permet de confirmer le diagnostic clinique et de trouver exactement quel est le problème. Toutes les mutations qui causent la DRH n’ont pas encore été identifiées, même si une grande partie est recensée. Quoi qu’il en soit le test génétique pourra vous en dire plus sur votre maladie.
Tests cliniques
Votre médecin ou ophtalmologue peut effectuer plusieurs tests différents pour diagnostiquer une DRH et déterminer de quelle forme il s’agit.
Qu’est-ce qu’un test clinique ?
- Un test du champ visuel : le but est de déterminer l’étendue de la dégradation de la vision périphérique. Grâce à un appareil non intrusif, des stimuli visuels sont envoyés et doivent être identifiés par le patient.
- Un imaginaire rétinien : utilisation d’une caméra spéciale pour capter les images situées derrière les yeux. Cela inclut les petites structures et les anomalies. Cette technique peut confirmer une suspicion de diagnostic clinique et aide à orienter les tests ultérieurs.
- Photographie du fond de l’oeil : c’est une photo de la rétine utilisée pour détecter des anomalies. Elle peut être combinée avec l’imagerie par auto-fluorescence pour avoir plus d’informations et également rendre le diagnostic de la maladie de Stargardt plus facile.
- Tomographie à cohérence optique : dispositif de lecture optique fonctionnant grâce à l’envoi d’ondes lumineuses rebondissantes sur la rétine. Cela permet d’avoir une représentation de ce qu’il se passe dans les couches de la rétine.
- Une électrorétinographie : mesure la réponse électrique des cellules des cônes et des bâtonnets grâces à des électrodes placées sur la cornée. Elle permet de voir si la cellule du photorécepteur fonctionne comme elle le devrait.
Tests génétiques
Qu’est-ce qu’un test génétique ?
Les tests génétiques impliquent une analyse de l’ADN, généralement grâce à un échantillon de sang et à un séquençage des gènes. Ainsi, il est possible de trouver des mutations spécifiques en lien avec votre DRH. Ce test est mis en place pour déterminer un diagnostic génétique à votre condition.
Pourquoi le test génétique est-il utile ?
Il peut aider à identifier exactement quelles mutations ont causé votre DRH. Il permet, entre autres, d’avoir une meilleure idée de comment votre maladie évolue et peut aider à sa prise en charge. Il est également possible d’identifier si vous pouvez être candidat pour un des essais cliniques ou un des traitements approuvés. Enfin, il peut fournir des informations qui guideront les prochaines recherches dans le traitement de la DRH.
D’autre part, il peut vous aider à vous sentir rassuré, vous renseigner sur la probabilité de transmission à vos enfants et vous permettre une meilleure prise en charge de votre maladie.
Comment être référencé pour le test génétique ?
Votre médecin ou ophtalmologue peut généralement vouloir identifier votre DRH par un test clinique avant de procéder à un test génétique. Il pourrait aussi vous demander de vous adresser à un conseiller en génétique avant de vous référencer pour un test de sorte à ce que vous puissiez être aidé et accompagné dans l’analyse de vos résultats.
Si vous pensez qu’un test génétique peut-être la meilleure option pour vous, parlez de cette possibilité à votre médecin.
107427 – Février 2021
Maladie rare d’origine génétique qui touche les motoneurones, cellules nerveuses qui servent à commander les muscles. Les muscles sont moins innervés (amyotrophie) et perdent de la force, entraînant des faiblesses musculaires qui touchent notamment la motricité, la respiration, la déglutition et l’articulation (parole).
En savoir plus sur l’amyotrophie spinale liée aux gènes SMN1 et 2 :
L’amyotrophie spinale (SMA: Spinal Muscular Atrophy) touche essentiellement les enfants, avec jusqu’à 100 nouveaux cas chaque année en France.
La SMA est liée à une anomalie génétique qui touche le gène SMN1, situé surle chromosome 5. Ce gène permet normalement la production de la protéine SMN (Survival of Motor Neuron), essentielle à la survie des motoneurones. Dans le cas de la SMA, le gène SMN1 est absent ou défectueux, ce qui conduit à la mort des motoneurones. Le nombre de copies du gène SMN2, qui est quasi-identique mais ne suffit pas à produire suffisamment de protéine SMN, influence la sévérité de l’atteinte.
Il existe ainsi 4 types d’amyotrophie spinale, en fonction de l’âge d’apparition des symptômes : type I, II, III ou IV, le type I étant la forme la plus sévère et de mauvais pronostic.
La maladie de Crohn est une maladie inflammatoire pouvant atteindre n’importe quel segment du tube digestif depuis la bouche jusqu’à l’anus. Elle est due à des anomalies du système immunitaire intestinal liées à un déséquilibre de la flore intestinale.
En France, la maladie de Crohn touche environ 1 personne sur 1 000, avec chaque année 8 nouveaux cas pour 100 000 habitants.
En savoir plus sur la maladie de Crohn
La maladie de Crohn est une maladie chronique qui se caractérise par des phases d’activité (ou « poussées ») d’intensité variable, alternant avec des phases sans symptôme dites de rémissions plus ou moins complète et prolongée.
Des complications peuvent survenir au cours de la maladie :
- un rétrécissement du diamètre intestinal (sténoses) ;
- des fistules (connexion anormale entre l’intestin malade et un autre organe ou la peau), des déchirures (fissures) et des abcès (infections).
Parfois, les symptômes de la poussée sont sévères, ce qui nécessite une hospitalisation.
Pathologie cancéreuse qui touche des cellules de la peau, appelées mélanocytes. Le mélanome se développe à partir d’une cellule normale, qui va se transformer et se multiplier de façon anarchique, pour former une lésion, appelée tumeur maligne. En 2018, 7 886 personnes ont été touchées par cette maladie.
En savoir plus sur le mélanome
Le mélanome représente 2 à 3 % de l’ensemble des cancers. C’est le cancer pour lequel le nombre de nouveaux cas par an (incidence) augmente le plus. Il existe 4 principaux types de mélanomes de la peau (superficiel extensif, de Dubreuilh, nodulaire et acrolentigineux). 80 % des mélanomes se développent à partir d’une peau saine, qui ne présente aucune tâche ou lésion. Les 20 % restant se développent à partir d’un grain de beauté existant.
Comment notre organisme se défend contre les aggressions
Les thérapies géniques et cellulaires utilisent souvent les systèmes de défense de notre organisme.
Découvrez en images quelles sont les cellules impliquées et comment fonctionne notre système immunitaire.